Introducción
El condroitín sulfato (CS) pertenece al grupo de los fármacos de acción sintomática lenta (SYSADOA, symptomatic slow acting drug for osteoarthritis) caracterizados por presentar una eficacia sobre los síntomas similar a la de los antiinflamatorios no esteroideos (AINE) que empieza de forma gradual pero se prolonga durante más tiempo incluso después de la supresión del tratamiento (efecto persistente o carry over). Asimismo se trata de productos de una gran seguridad.
Los ensayos clínicos en pacientes artrósicos demuestran que el tratamiento con CS produce una disminución o desaparición de los síntomas de la enfermedad artrósica, como son el dolor y la impotencia funcional, mejorando el movimiento de las articulaciones afectadas, con un efecto que perdura 2 o 3 meses.
Dado que se trata de un fármaco de acción sintomática lenta (SYSADOA), el inicio de acción de CS es algo lento, entre 2-3 semanas, aunque eventualmente alcanza la misma eficacia que los antiinflamatorios.
Material y métodos
Para determinar la eficacia del CS en el tratamiento sintomático de la artrosis se han realizado varios ensayos clínicos que ponen de manifiesto su utilidad para dicha afección. A continuación se resumen las evidencias clínicas disponibles con CS.
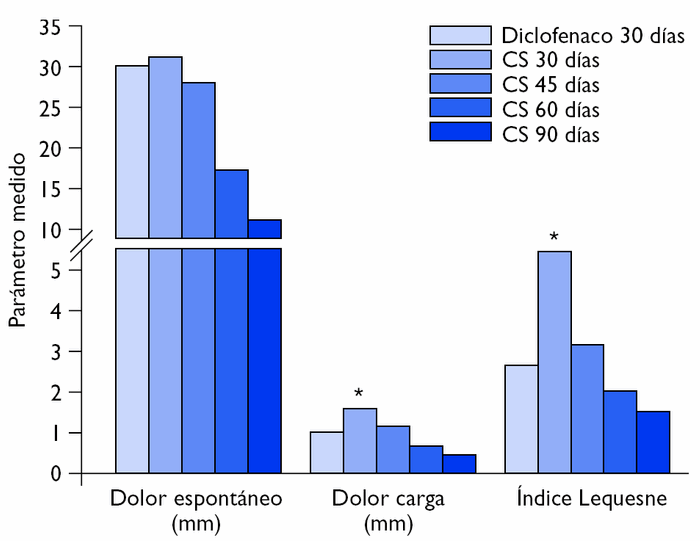
Se ha realizado un ensayo clínico aleatorizado, multicéntrico, a doble ciego con 146 pacientes con artrosis de la rodilla de 6 meses de duración, comparando el diclofenaco sódico (DS) tomado durante 30 días frente al CS tomado durante 90 días1. Los resultados se resumen en la figura 1.
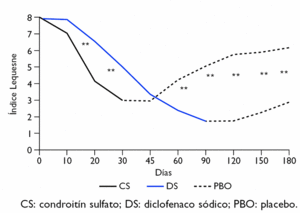
Figura 1 Efecto antiálgico y funcional del diclofenaco sódico, 150 mg/día durante 30 días, y del condroitín sulfato (CS) 1.200 mg durante 90 días, medidos a los 30, 45, 60 y 90 días. *p < 0,05 frente al diclofenaco.
Teniendo en cuenta únicamente las medidas de dolor y funcionales a los 30 días de tratamiento, puede concluirse que el CS disminuye el dolor espontáneo con la misma eficacia que el DS. Sin embargo, a los 30 días de tratamiento, el efecto del CS sobre el dolor a la carga y sobre el índice Lequesne es inferior al alcanzado con DS.
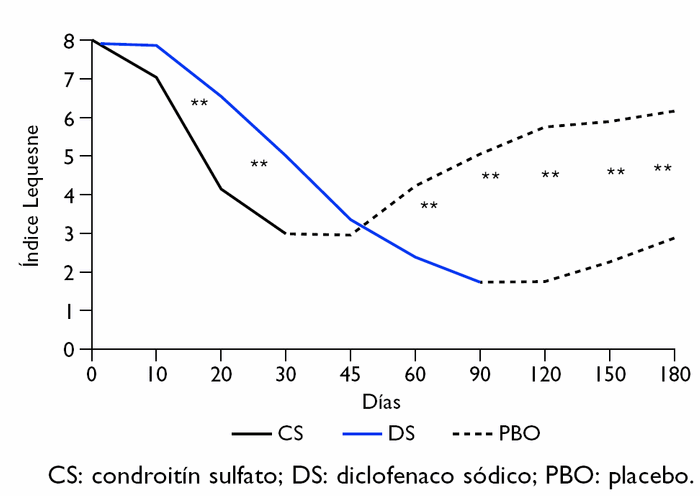
A partir del día 45 de estudio, el efecto del CS fue semejante al del DS. No obstante, durante los meses cuarto, quinto y sexto, cuando los pacientes sólo tomaron placebo, el efecto disminuyó significativamente en el grupo del DS, mientras que el grupo del CS mantuvo su efecto positivo. Al cabo de los 6 meses, la puntuación en el grupo del CS fue un 64,4% inferior a los valores iniciales, y la del grupo del DS, un 29,7% (fig. 2).
Figura 2 Valores medios del índice Lequesne durante el estudio.
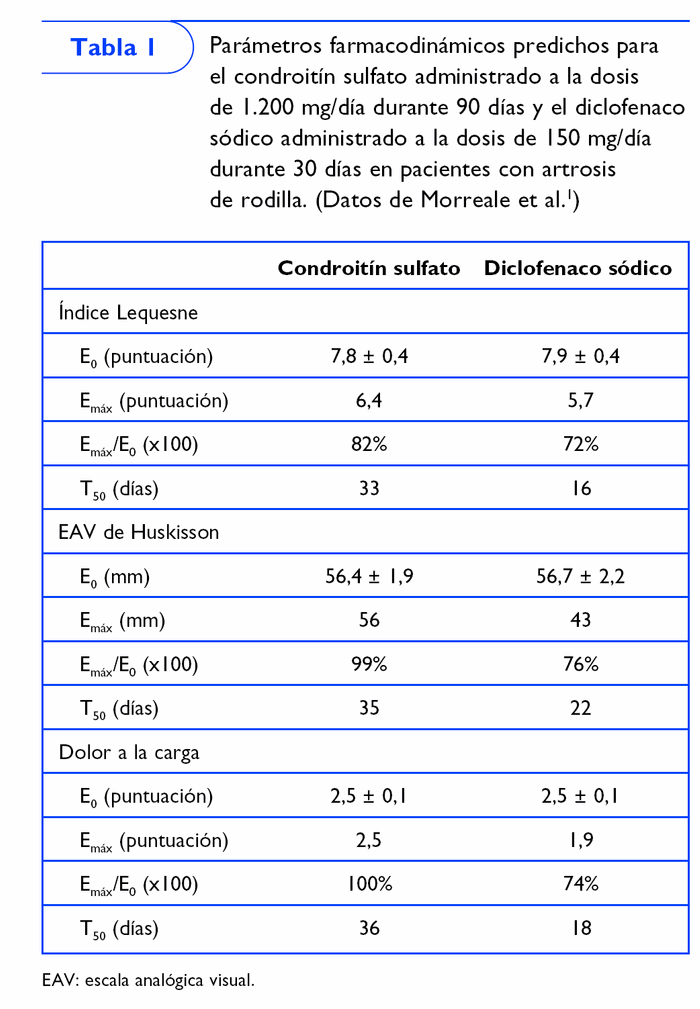
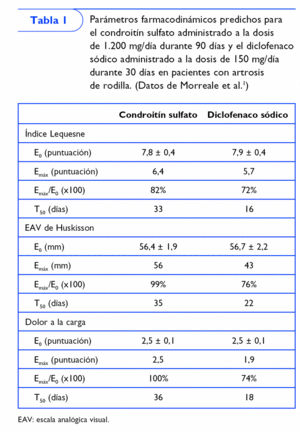
Otro estudio2 ha definido las características de la respuesta del CS durante y después de su administración, tomando como referencia el efecto de 150 mg de DS. Para este fin, se evaluaron varios ensayos clínicos aleatorizados, a doble ciego, controlados con placebo, que incluían pacientes con artrosis de rodilla.
El efecto del CS sobre el estatus funcional (índice Lequesne), el dolor espontáneo (escala analógica visual [EAV] de Huskisson) y el dolor a la carga fueron evaluados utilizando el modelo Emax. Esta metodología permite predecir el efecto máximo obtenible (Emáx), y el tiempo requerido para obtener el 50% de la Emáx (T50).
Resultados
Los resultados de este estudio (tabla I) sugieren que la respuesta más favorable predicha en pacientes con artrosis de rodilla que han recibido 800 mg/día de CS durante 90 días es ligeramente superior a la predicha para el DS, aunque el CS tarda el doble en conseguir el efecto más favorable. No obstante, el efecto remanente del CS persiste el doble que el del DS.
En total, 9 ensayos clínicos, aleatorizados, a doble ciego, han comparado el efecto del CS con el del placebo en pacientes con artrosis de rodilla y dedos, tratados durante períodos que oscilaron entre 3 y 36 meses.
Los resultados de todos los ensayos clínicos coinciden en concluir que el CS es más eficaz (aproximadamente el 50%; p < 0,05) que el placebo en reducir el dolor espontáneo, aumentar la capacidad funcional, disminuir la ingesta de medicación de rescate y en la valoración global del paciente y el investigador.
Asimismo, un metaanálisis3 recoge los datos de 7 ensayos clínicos suficientemente homogéneos como para ser analizados conjuntamente. Un total de 703 pacientes fueron incluidos en estos ensayos clínicos, 372 tratados con CS y 331 con placebo. El efecto del CS sobre el dolor espontáneo y sobre la capacidad funcional fue significativamente superior al placebo a partir de los 4 meses. Las evaluaciones realizadas por los pacientes y los médicos demuestran que el tratamiento con CS es superior al placebo. Finalmente, los pacientes tratados con CS tomaron significativamente menos medicación de rescate que los pacientes que reci-bían placebo. Además, se destaca que los efectos adversos fueron leves y más elevados en los grupos placebo que en los de CS.
Cabe destacar un nuevo y reciente ensayo clínico4 (GAIT, Glucosamine/Chondroitin Arthritis Intervention Trial) multicéntrico, aleatorizado y doble ciego en un total de 1.583 pacientes con artrosis de rodilla, en el que se estudió el efecto de 5 tratamientos (500 mg de glucosamina 3 veces al día; 400 mg de CS 3 veces al día; 200 mg de celecoxib al día; 500 mg de glucosamina + 400 mg de CS 3 veces al día; placebo) sobre la reducción del dolor durante 6 meses.
En este ensayo clínico se observó una disminución significativa de la hinchazón, acompañada o no de derrame articular (sinovitis), en el grupo tratado con CS, comparado con placebo (p = 0,01).
Clegg et al5, basándose en el mismo estudio (GAIT), también evaluaron si el CS podría tener un efecto diferencial sobre los síntomas de la artrosis en cuanto al grado radiográfico de Kellgren & Lawrence (KL) de los pacientes. Los resultados sugieren que el CS podría mejorar el dolor de la artrosis de rodilla en pacientes con fases iniciales de la patología, en concreto con grado 2 de KL.
Conclusión
En definitiva, podemos concluir que el CS es una herramienta terapéutica de gran utilidad para el tratamiento de la artrosis.
Correspondencia:
Josep Vergés.
BIOIBERICA, S.A.
Plaza Francesc Macià, 7.
08029 Barcelona. España.
Correo electrónico: jverges@bioiberica.com